最新フッ素関連トピックス」はダイキン工業株式会社ファインケミカル部のご好意により、ダイキン工業ホームページのWEBマガジンに掲載された内容を紹介しています。ご愛顧のほどよろしくお願いいたします。尚、WEBマガジンのURLは下記の通りです。
http://www.daikin.co.jp/chm/products/fine/backnum/201209/#topic01
1、はじめに
クロスカップリング反応とは、二つの異なる化学物質を選択的に結合させる反応のことで、有機ホウ素化合物を用いる鈴木‐宮浦反応、溝呂木‐Heck反応、根岸反応などがあるが、鈴木氏、根岸氏のノーベル賞受賞は記憶に新しい。今回は、本反応にフッ素がどう関わっているかとの観点に立って、最近の情報を提供する。
2、有機フルオロホウ素錯体1)
有機トリフルオロホウ素錯体(RBF3K)は、一般に広く鈴木-宮浦反応に用いられる有機ボロン酸またはボロン酸エステルに比して高い結晶性を有し、空気に対する安定性が高いため取扱が容易である。その合成法を下式に示す。フッ素化剤としてKHF2を用いたことがこの錯体の分野を大きく進展させた。

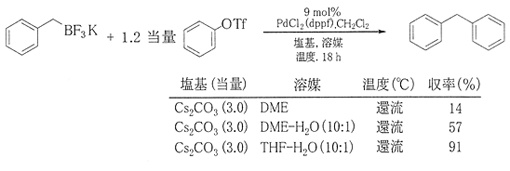
ArBF3Kを用いたカップリング反応の例として下式を挙げる。この場合、パラジウム触媒反応であり、CsCO3のような塩基および水の添加が必要であった。
また、溶媒の影響も大きいことが分かった。
3、含フッ素N-ヘテロ環状カルベン2)
下記の6aで示される含フッ素N-ヘテロ環状イミダゾリウム化合物とパラジウム錯体を組み合わせた触媒は鈴木ー宮浦反応を促進する。この場合、フッ素を含まない種々のイミダゾリウム化合物と比較していて、フッ素の効果は明白である。
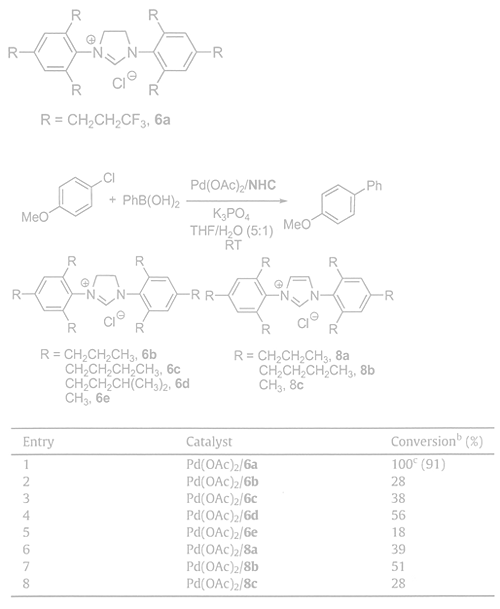
この場合、Pd(OAc)2とイミダゾリウム化合物はそれぞれ3モル%と6モル%であり、塩基としてK3PO4 2.8mmol、溶媒としてTHF/水(5/1)が使用され、室温で3時間反応させている。bはガスクロマトグラフィーにより決定、カッコ内は単離収率である。
4、フルオラス配位子を有する金属錯体3)
4-1フルオラス溝呂木‐Heck反応
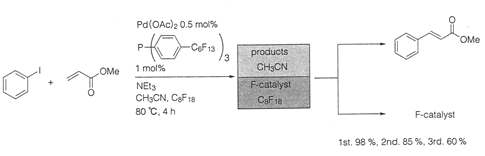
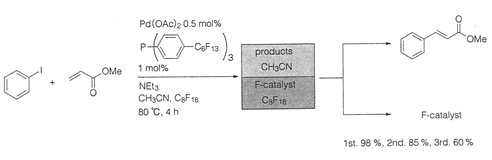
下図に示すパラジウム触媒存在下で有機ハロゲン化合物と末端アルケンから内部アルケンやスチレン誘導体を合成する溝呂木‐Heck反応において、フルオラスPd触媒を用いると高い収率で生成物が得られる。この場合、生成物は有機溶媒相へ、フルオラス触媒はフルオラス相へ分配され、それぞれ単離が容易であり、触媒はリサイクルできる。
4-2フルオラス鈴木‐宮浦反応
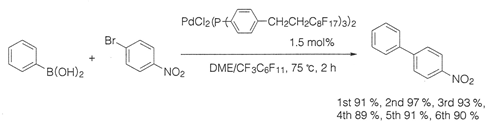
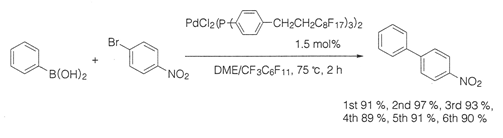
フルオラス化したホスフィンを導入したPd触媒による鈴木‐宮浦反応を下図に示す。反応はジメチルエーテル(DME)/パーフルオロメチルシクロヘキサンCF3C6F11の2相系で行い、回収した触媒系を用いて数回反応を繰り返し、高い収率を得ている。
5、含フッ素化合物の鈴木‐宮浦反応による合成
特にバイオ有機化学において注目されているフッ素を含む化合物の合成に鈴木‐宮浦反応を利用した例を最後に紹介する。まずは、抗がん剤、抗ウイルス剤として有用である含フッ素ヌクレオシドの合成である。4)下記に示すのは5-(ジヒドロキシボリル)‐2,4-ビスアルコキシ‐ピリミジンとフルオロアルケンとの鈴木ー宮浦反応による合成法である。ここでbは、Pd(PPh3)4/AsPh3触媒、THF溶媒、2M KOH、65~70℃の反応条件を示す。R1、R2、R3がFでRがC2H5の時、収率は65%であり、Rがt-Buの時は45%であった。
次いで、プロパギルフルオライドとアセタアミジンとの反応によるモノフッ素化アルキル基を含有するパラブロモフェニルピリミジンとアリールボロン酸との鈴木ー宮浦反応による含フッ素ピリミジン誘導体の合成法を下記に示す。Arがフェニルの場合82%の収率であった。本方法は、生理活性物質として期待される含フッ素ピリミジン誘導体の合成法として期待される。5)
6、おわりに
鈴木ー宮浦カップリング反応を中心としてカップリング反応にフッ素がどう関与しているかを概観した。改めてこの反応が工業的に広く用いられ、また化学的な興味の対象になっているかを認識できた。そして、フッ素は触媒としてユニークな係わり合いを持ち、重要な位置付けを得ていること、さらにはこの反応で合成されたフッ素化合物がバイオの分野をはじめとして有用であることも知ることができた。今後もこの反応とフッ素の係わり合いに目が放せないと感じている。
文献
1) 伊藤貴敏 科学と工業86(4) 127-134 2012
2) Long Lu et al Tetrahedron 68(32) 1-13 2012
3) 「クロスカップリング反応」シーエムシー 2012
4) Hanna Wojyowicz-Rajxhel et al J. of Fluorine Chemistry 135(2012) 225-230
5) Pierre Wanbarth et al J. of Fluorine Chemistry 134(2012) 180-187