最新フッ素関連トピックス」はダイキン工業株式会社ファインケミカル部のご好意により、ダイキン工業ホームページのWEBマガジンに掲載された内容を紹介しています。ご愛顧のほどよろしくお願いいたします。尚、WEBマガジンのURLは下記の通りです。
http://www.daikin.co.jp/chm/products/fine/backnum/201303/#topic01
1、はじめに
電池関連の最新トピックスは2010年12月に「電解質に使用されるフッ素化合物」と題して述べている。ここでは、それ以降の電池関連フッ素系材料の進展状況について述べる。
2、電解質
久保田らは、電荷、高電圧リチウムイオン電池の電解質添加剤として、下図に示す1,1-ジフルオロ-1-アルケン類を検討した。1)目的は好ましい固体電解質界面(SEI)の形成に導くことである。
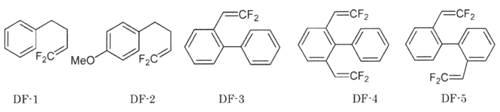
この中で、DF-1が、酸化還元条件で、正極、負極上に適切なSEI形成を示し、サイクル特性が優れていた。それはDF-1が他のアルケン類より反応性が低く、最初のサイクルでSEI形成が終了することからくる。X線分析の結果、正極にはLiFリッチの層が生成していた。さらに負極もLiFリッチの層が生成していた。この結果は、高容量リチウムイオン電池、新規電解質添加剤の分子設計のガイドラインを示すものとして期待できるとしている。
リチウムイオン電池における電解液溶媒としてはプロピレンカーボネートPCが使用されているが、負極のグラファイトとの適合性が低く、グラファイト構造を破壊することが起きている。その対策として、Martin Winterらは電極間物質(SEI)を形成させる物質として1-フルオロプロパン‐2-オン(フルオロアセトンFA)を検討し、そのSEI形成機構を調べた。2)電解液として、PC98%、炭酸ビニレン(VC)1%、FA1%、1MLiPF6を用いた。NMR、Raman、XPSスペクトルを駆使して解析した結果、下記のSEI形成機構を提案している。
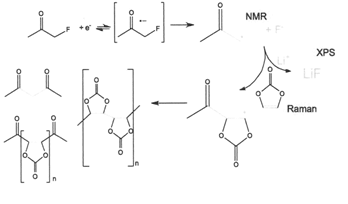
即ち、NMRにより電解質中でC-F結合が減少していくことを捕らえ、XPSでグラファイト負極にFイオンが高濃度で存在することが分かり、Ramanスペクトルで炭酸ビニレンが減少していくことが分析された。
リチウムイオン二次電池の安全性を改良すべく、不燃性のイオン液体を使用する開発がなされているが、大野らは現行のエチレンカーボネート/ジメチルカーボネートの系(LP30)にイオン液体N-n-ブチル-N-メチルピリジニウムヘキサフルオロフォスフェート[Py14]PF6とP(VDF-HFP)を加えた高分子電解質を提案している。3)イオン液体をLP30に対して30%加えた系がより優れた電池特性を示すと同時に高い熱安定性を示した。
3、電極材料
LiFePO4Fがリチウムイオン電池(LiB)のカソードとして期待されている。現在、LiFePO4(OH)は3LiBのカソードとして使用されているが、LiFePO4FはLiFePO4(OH)に比して熱安定性が高く、電極電位も2.6Vに比して2.75Vと高い。M.V.Leddyらは、LiFePO4FをFePO4とLiFとの固体反応で合成し、構造や表面積、電気化学的特性を調べた。4)その結果、イオン電導性は、27℃で0.6×10‐7Scm-1、50℃で5.4×10-7cm-1であり、その際の活性化エネルギーは0.75eVであった。また、充放電特性としては初期放電容量が115mAhg-1であったものが20サイクル目まで少しずつ上昇し、119mAhg-1となった。その後、減少に転じ、100サイクル目では、96mAhg-1となった。サイクリックボルタンメトリー測定により、2層Li相間脱離挿入反応が起こっていることが分かった。
Katia Guёrinらは、フッ素化カーボンとナノカーボンのリチウム一次電池の電極物質としての電気化学的性能として、フッ素化カーボンを陽極として、エネルギー密度を評価した。その結果をFig.1に示す。フッ素ガスで後フッ素化するとエネルギー密度が温度とともに上昇し、500℃で最大になる。そして、600℃以上になると急激に低下することが分かった。5)
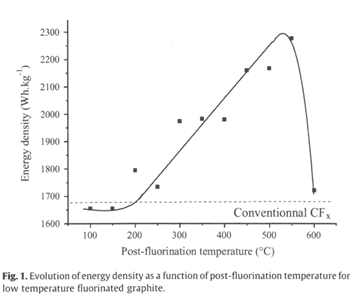
現在、リチウムイオン二次電池(LiB)の正極活物質には、LiCoO2、LiMn2O4やLiFePO4などの化合物が使用されており、そのエネルギー密度は500Wh/kg前後であり、さらなる高容量化が望まれている。フッ化鉄やフッ化マンガンのような遷移金属フッ化物についても、正極活物質への応用が検討されており、中でもフッ化鉄FeF3は、高容量を達成できる化合物として有望視されている。FeF3の結晶構造は欠陥ベロブスカイト型構造であり、LiイオンやNaイオンなどをその欠陥サイトに可逆的に挿入でき、その脱離挿入反応のみで700Wh/kgを超えるエネルギー密度が期待できる。さらに、Feイオンを金属にまで還元する反応を利用することで、1100Wh/kgを超えるエネルギー密度が期待できる。しかし、電子伝導性に乏しく、活物質としての特性を引き出すためには導電性カーボンとのコンポジット化などの手法が必要である。また、FeF3は吸湿性であり、大気中での取扱が困難であるなどの問題点がある。富田は、FeF3表面を酸化することで大気中の安定性を向上し、加えてLi脱離挿入反応を利用した正極活物質としての特性を改善した。6)
4、ナトリウム電池
ナトリウムイオン電池はリチウムを用いないレアメタルフリー構成を実現する電池として期待されている。
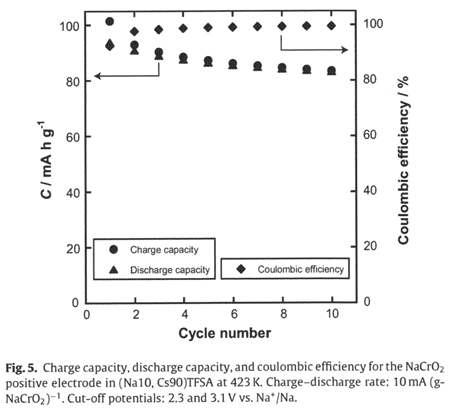
萩原らは、423Kで作用するNaCrO2を正極とするナトリウム二次電池における新電解質として、イオン液体NaTFSA(10mol%)/CsTFSA(90mol%)を検討した。7)このイオン液体の423Kでの粘度、イオン伝導度、密度、電気化学窓はそれぞれ、42.5cp、12.1mS/cm、2.29g/cm-3、4.9Vであった。本条件での充放電特性を調べ、定電流速度が10サイクル後10mA/gの場合と50サイクル後100mA/gの場合における放電容量はそれぞれ83.0mAh/g、66.4mAh/gであった。初期の数サイクルを除くとクーロン効率は99.5%以上であった。このことから、このナトリウム二次電池が423Kを中心とする373Kから473Kの温度範囲で新規二次電池として有望であるとしている。
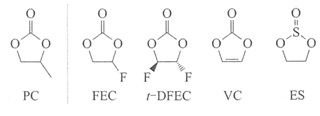
駒場は、ナトリウムイオン電池において、正極・負極の長寿命化を目指した電解液添加剤に関する論文を発表している。8)電解液添加剤は負極上に不動態皮膜(SEI)を生成させることを目的としてリチウムイオン電池では一般的に使用されている。SEIはリチウムイオン電池においてカーボン負極上に精製して保護皮膜として働くことはよく知られている。この皮膜がナトリウムイオン電池においても存在することを確認している。但し、SEI皮膜の主成分はリチウムイオン電池の場合と異なり、無機化合物であることも確認している。リチウムイオン電池同様、電解液添加剤によりSEIが生成するかについて検討した。その結果、下図に示す添加剤をPC電解液に添加した場合、FECのみが電解液量が限られるコイン型セルを用いた場合でも、80サイクルにわたって200mAg-1以上の充放電が可能であった。
結論として、正極にNa2/3Fe1/3Mn2/3O2を、負極にハードカーボンを用い、電解液として1M NaPF6/PC:FEC(体積比99.5:0.5)を使用したナトリウムイオン二次電池において、3V級の電池作動に成功した。50サイクル後も約7割の蓄電量を維持しており、将来的には高エネルギー密度を有する長寿命なナトリウムイオン二次電池として利用されることが期待されるとしている。
岡田らは、Na3M2(PO4)2F3[M=Ti, Fe, V]を2段階固体状態合成で合成し、ナトリウムイオン電池の負極活物質としての可能性を調べた。9)合成は、V2O5あるいはTi2O3と(NH4)2HPO4とを混合し、650~950℃15時間熱するか、FePO4・2H2Oを100℃、真空中で3時間熱してMPO4の形にし、次いで、NaFと混合して空気流の中で600℃2時間反応させた。Na3V2(PO4)2F3が容量として120mAであり、サイクル特性も20サイクル後の保持率が98%と高く、安定していることがわかった。
5、おわりに
リチウム二次電池における企業の動きは活発化している。例えば、三菱化学とステラケミファ、宇部興産とダウ・ケミカル、森田化学と住友商事が提携を結び体質を強化している。BASFは世界3極に電解液生産拠点を築き、宇部興産はLiB電解液事業において日・米・欧3極で3万トン体制を構築した。ダイキン工業はLiB電解液に参入、まず米工場に2000トン設備を建設し、電解質内製化を図り、フッ素技術生かし差別化し、米中などで量産を計画している。
また、LiBは民生用の小型分野の普及が進んできたが、今後は車載や電力貯蔵用の大型分野での需要拡大が期待される。大型LiBは高温下での長時間使用が求められ、電解液の分解による電池の内圧上昇・破裂や溶媒の漏洩や噴出などによる発火への備えが重要課題となっている。最近のリチウム電池が原因の航空機におけるトラブルは記憶に新しい。今後はさらなる高性能化、高安全性やリチウムを用いないナトリウム電池の開発が加速され、フッ素系材料の役割はますます重要性を増していくと考えている。
文献
1) Tadahiko Kubota et al Journal of Power Sources 207(2012) 141-149
2) Martin Winter et al Electrochimica Acta 81(2012) 161-165
3) Hiroyuki Ohno et al Journal of Power Source 233(2013) 104-109
4) M.V. Leddy et al Electrochimica Acta 85(2012) 572-578
5) Katia Guёrin et al Journal of Fluorine Chemistry 134(2012) 11-17
6) 富田靖正 ケミカルエンジニヤリング 2012年8月号45-49
7) Rika Hagiwara et al Journal of Power Sources 205(2012) 506-509
8) 駒場慎一他 ファインケミカル41(8) 22-28 2012
9) Shigeto Okada et al Journal of Power Sources 227(2013) 80-85