最新フッ素関連トピックス」はダイキン工業株式会社ファインケミカル部のご好意により、ダイキン工業ホームページのWEBマガジンに掲載された内容を紹介しています。ご愛顧のほどよろしくお願いいたします。尚、WEBマガジンのURLは下記の通りです。
http://www.daikin.co.jp/chm/products/fine/webmaga/201707.html
1、はじめに
リチウムイオン電池(LiB)は、現在最も高い能力を有する電池であり、携帯電話、電気自動車(EV)、大規模電気化学貯蔵などに使われている。電池の容量をさらに上げる努力は続けられており、その候補の一つとして、フルオライドイオン(F‐)を電荷移動体とするフルオライドイオン電池(FIB)がある。F‐は非常に安定であり、広い電気化学窓を有しているので電池の電荷移動体として高いポテンシャルを持っている。
2、FIBの作用理論と理論性能1)
下記にカソードとしてBiF3、アノードとしてMgを用いた電池を示す。

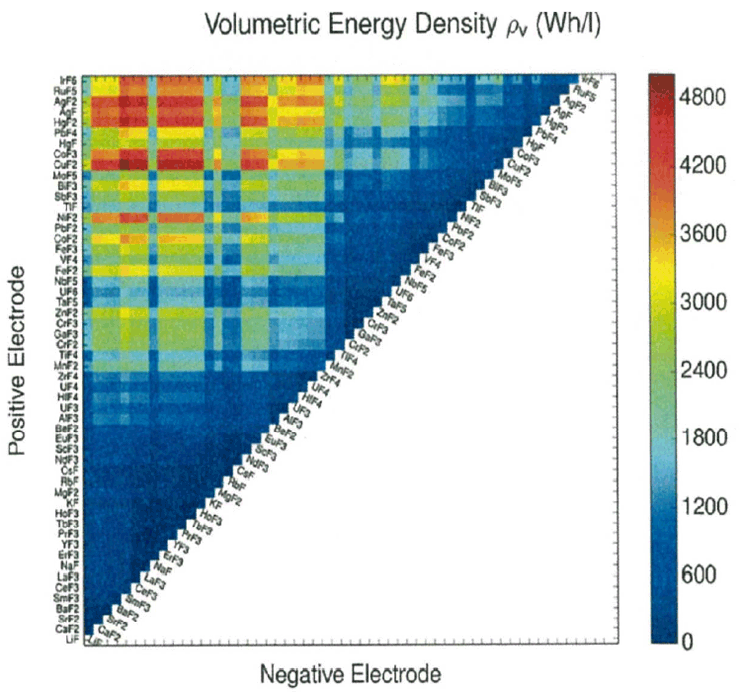
理論的に、各電極で起こっている反応をもとに、MFxとM’Fyの化学ポテンシャルの差から無負荷電圧を計算し、重量電気容量および体積エネルギー密度(下図)を求めている。体積エネルギー密度は色分けされていて右の棒グラフにその値が示されている。この図から、正極としてAgF2、CoF3、CuF2、NiF2、IrF5など、負極としてCeF3、LaF3、IrF3、YF3、PrF3、など130のFIBs系がLIBより高い性能を有している。(LiBでは1015Wh/l)
3、FIBの種類
FIBには、全固体FIB(高温FIB、HTFIB)と液体電解質で、室温で作動するRTFIBがある。
HTFIBは、アノードにCeF3、カソードにBi、電解質としてLa0.9Ba0.1F2.9(CeF3/ La0.9Ba0.1F2.9/Bi)を用い、4Vで充電容量400mAh/g が得られた。Bi2O3がフッ素化されたBiOF、BiF3_2xOxが観測されている。放電容量は20mAh/gと低く、臨界電圧は2.3Vであった。Mg・MgF2/ La0.9Ba0.1F2.9/Cuでは充電容量266mAh/g、放電容量88mAh/gでサイクル数は10回であった。HTFIBの課題は充放電中に体積変化が起こり、電極物質が破壊すること。対策として、タイソン石薄膜を導電層として使用し、厚い電解質フィルムによりイオン伝導抵抗を低減している。
RTFIBは、フリーのF-あるいはHF2-イオンを確保しなければならない難しさがある(すぐにHFになってしまう)。カソードとしてBiF3、アノードにLiあるいはMgを用い、電解質NH4+HF2-をPEGにドープNH4+PEGカチオンが形成され、HF2-が電荷移動体となり、PEGとして分子量194~200,000を検討している。分子量が低い方が高性能であった。250℃までF-は確保できた。イオン電導度1000μS/cmと低く、電気化学窓も狭く、サイクル回数も0。そこで、カソードとしてBiF3、AlF3、CuF2、TiF3 アノードとしてLi、Mg、Naを選定し、その組み合わせの研究が行われている。1)
4、薄膜電極電解質
Maximilian Fichtnerらは、下図(a)のバルク型電池を作製。初期は理論値の70%の性能が達成され、充放電サイクルは700μmの厚い電解質層の抵抗が大きく、また電極と電解質間の接触が不十分なため抵抗が増大し、容量低下が大きかった。そこで(b)に示す薄膜電極電解質を提案。ゾルゲルスピンコーティングで得た膜厚5~6μmLa0.9Ba0.1F2.9薄膜が170℃で8.8×10-5S/cmの電導度を示した。2)

また、La0.9Ba0.1F2.9溶液をスピンコーティング、400、450、500℃で0.5~4時間シンタリングを行った。その中で450℃、4時間かけてシンタリングした4~5μmの薄膜は170℃で1.6×10-4S/cmで最も高いイオン伝導度を示した。3)
Damien Dambournetらは、固体状態二次FIBについて、Bi/BiF3電極のコインセルを修正して、グローブボックスの外で高温下長時間の電気化学的性質を調べている。4)150℃に熱したエポキシ樹脂でコインセルを覆い、結果としてセルをシールしたことになった。3サイクル後190mAh/gの容量が得られた。
Xiangyang Zhouらは、電極とセパレーターの間にセルロース紙上にコートした多孔性カーボンとグラフェンからなる中間層を導入し、FeF3・0.33H2Oのナノ粒子電極で、250サイクル後に放電容量435mAhr/gを達成した。5)
5、特許に見るFIB
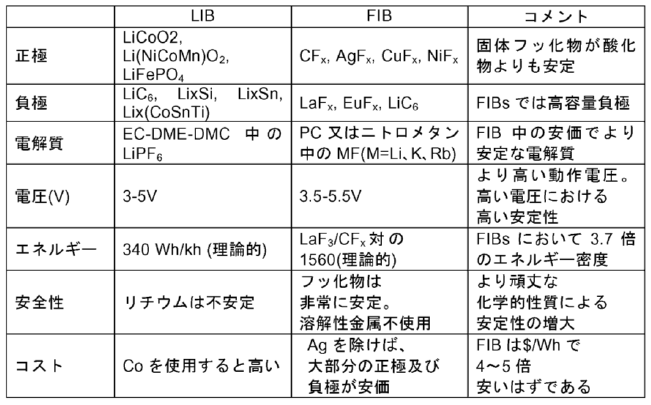
カリフォルニア・インスティテュート・オブテクノロジーはフルオライドイオン電池(FIB)を検討し、LiBとの違いを表にまとめている。6) FIBの利点には、フッ化物イオン電気化学セルの安全性の向上、フッ化物イオン電気化学セルのより高い動作電圧、フッ化物イオン電気化学セルにおけるより大きいエネルギー密度、及びフッ化物イオン電気化学セルのより低いコスト、が含まれる。
アニオン受容体として、B(OCH2CF3)3などのホウ素化合物が提案され、フルオライドイオンの溶解度を高めるのに必須であるとしている。具体的にはLa3-xを負極に、CFxを正極とする例が示されている。
京都大学はトヨタ自動車と共同で、FIBに関する特許を公開している。
まずは電解液に関する特許で、CsFを含むLiTFSAテトラグライム溶液 7)、LiFやNaFを含むLiPF6あるいはLiBF4テトラグライム溶液あるいはトリグライムとLiPF6とのモル比が8以下の溶液(モル比が10以上になるとLiイオン電池になる)8)、フッ化物錯アニオンを含むイオン液体(N-ブチルピリニジウムBF4)とB(C6F5)3のようなアニオン受容体の溶液9)などが提案されている。
次いで、負極活物質としてCeあるいはPbを含む合金を使用して充電時の過電圧を低減した(電解液はテトラグライム/LiTFSA/CsF)。10)
さらに負極集電体として、Fe、MgあるいはTiの単体、または、これらの金属元素の1つ以上を含有する合金を用いて、電解液(テトラグライム/LiTFSA/CsF)との反応を抑制した。11)
また、京都大学は日立製作所とも以下の内容の特許を公開している。12)BiF3、PbF2あるいはSnF2を電極活物質とし、(C9H11)2BFなどのホウ素化合物及びCsFなどのアルカリ金属のフッ化物塩を含む電解液とを備えた、現行の電池を超える高容量のフルオライドイオン電池を提案している。
さらに、京都大学は本田技研工業ともイオン伝導率に優れ、フッ化物イオン2次電池の固体電解質として十分な電気特性を示す結晶体の製造方法、結晶体及びフッ化物イオン2次電池用電解質を提供するという特許を公開している。13)PbF2とSnF2を混合し、不活性雰囲気において混合物の融点以上の温度で焼成することにより結晶体を作製し、フッ化物2次電池用電解質として解決している。
6、おわりに
フルオライドイオン電池は理論的には現行のリチウムイオン電池より数倍のの容量が期待されるが、プロトンとの反応によりHFになってしまうこと、薄膜にしないと抵抗が大きく特に充放電サイクル特性が低いことなどまだまだ実用化にはかなり遠い感じがする。京都大学はトヨタ自動車や日立製作所などと共同で本電池の実用化に向けて地道な努力を続けている。このポテンシャルの大きさを実用化に結び付けるべく、難題を克服して進化していくことを期待したい。
文献
1) F. Gschwind et al J. of Fluorine Chemistry 182(2016) 76
2) Maximilian Fichtner et al Solid State Ionics 272(2015)39
3) Maximilian Fichtner et al J. of Alloys and Compounds 684(2016) 733-738
4) Damien Dambournet et al J. of Fluorine Chemistry 191(2016) 23-28
5) Xiangyang Zhou et al Electrochimica Acta 220(2016) 75-82
6) カリフォルニア・インスティテュート・オブテクノロジー 特開2013-145758
7) トヨタ自動車、京都大学 特開2016-062821
8) トヨタ自動車、京都大学 特開2016-197543
9) トヨタ自動車、京都大学 特開2016-164857
10) トヨタ自動車、京都大学 特開2017-050113
11) トヨタ自動車、京都大学 特開2017-054721
12) 日立製作所、京都大学 特開2017-10865
13) 本田技研工業、京都大学 特開2017-88427