最新フッ素関連トピックス」はダイキン工業株式会社ファインケミカル部のご好意により、ダイキン工業ホームページのWEBマガジンに掲載された内容を紹介しています。ご愛顧のほどよろしくお願いいたします。尚、WEBマガジンのURLは下記の通りです。
http://www.daikin.co.jp/chm/products/fine/webmaga/201609.html
1、はじめに
ドラッグデリバリーシステム(DDS)とは、体内の薬物分布を量的・空間的・時間的にコントロールする薬伝達システムのことである。薬の過剰投与および副作用を抑制して、より安全に、効果的にドラッグ投与を行うことができる。このDDSにフッ素がどうかかわっているのかについては2013年7月号で取り上げているので、今回はその後の動きについて述べる。その時はDD方式としてカプセル化とエアゾール化を取り上げ、フッ素の役割として、ドラッグを取り込む場合の効率化とドラッグを放出する場合の徐放性、さらには19FNMRによる画像化ができることを述べた。今回は、まずは、DDSについての最近の文献からその概要を述べる。次いでフッ素が関与するDDSとして、抗がん剤や合成抗菌剤などに使用されるフッ素系医薬のデリバリーシステムやDD物質としてのフッ素化合物、DDSの代謝安定評価に19FNMRを用いた例などを紹介する。
2、DDSの概要
薬物の体内動態を量的、空間的、時間的に制御するDDSの概念が登場してから40年経過していて、現在では多くのDDSが医療現場で使用されている。DDSはその目的に応じて、吸収改善、放出制御、ターゲティングの3つに分類される。
まず吸収改善であるが、薬物の吸収性は薬物と吸収障壁、さらにはこの両者に影響を及ぼす製剤との相互作用により決定される。そして、吸収改善は薬物の修飾、吸収障壁の克服、投与経路の変更の3つに大別される。1)このうち薬物の修飾は、薬物分子の修飾と薬物剤形修飾があるが、前者は、薬物に脂溶性の官能基を付加することにより膜への分配性を高め、透過性を促進する方法である。後者は主に溶解性(溶解速度と溶解度)が鍵となるが、溶解速度については薬物粒子の微細化であり、ナノスケールにまで微細化されて製品化されている。溶解度についてはアモルファス化することが有効で薬物を水溶性高分子に分子分散化し、安定的にアモルファス化した例がある。また、溶解性を上げる方法として界面活性剤による可溶化の手法がある。
放出制御とは、薬物を製剤から種々の速度で放出し、薬物の有効性の持続化のみならず、投与初期の急な薬物濃度の高まりを抑えて副作用を軽減し、投与回数を少なくし利便性を高めることである。その中で徐放化DDS技術が最も汎用されている。放出制御のメカニズムとしては、製剤表面に形成された膜の溶解および膜中の拡散律速によって放出が制御される膜制御、薬物結晶を高分子基剤中に懸濁した状態にしておき、飽和溶解度に依存した一定速度の放出が得られるマトリックス制御、浸透圧物質を製剤中に共存させ、その浸透圧により一定速度で放出する浸透圧制御、例えばpHの変化、熱、電磁波、超音波、レーザー光の照射などによって薬物を含有するポリマー構造が変化し薬物放出が加速される現象を利用した外部刺激応答性制御などがあり、それぞれの制御メカニズムを利用した放出制御製剤が使用されている。2)
ターゲティングについては、パッシブ・ターゲティングとアクティブ・ターゲティングの2種類ある。パッシブ・ターゲティングは、薬物運搬体(キャリアー)の粒子径や親水性などの物理化学的性質を利用して薬物の体内動態を制御する方法。アクティブ・ターゲティングは、薬物運搬体に、特殊な仕組み(たとえば、抗体や糖鎖などを結合したキャリアーを利用)を付け加えて標的組織への指向性を制御する方法である。
最後にDDSに使われる材料であるが、薬物以外の素材としては、無機・有機化合物、低分子・高分子化合物の多岐にわたるが、実際には多くが有機化合物であり、さらにそのほとんどがポリマーである。そのポリマーとしては、多糖類、ペプチド、たんぱく質、核酸などの天然ポリマー、生分解性の合成高分子などが使用されている。材料の形態としては可溶性ポリマー、可溶性(コロイド状)微粒子、不溶性微粒子、ゲル状のものなどがある。使用実績のあるポリマーとしては、デキストラン、キチン、ヒアルロン酸、ゼラチン、アクリル系ポリマー、スチレン/マレイン酸共重合体、ポリエチレングリコール、ポリエチレンイミン、ポリ乳酸、ポリデプシペプチドなどである。3)
3、フッ素系医薬のデリバリーシステム
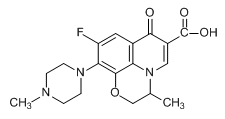
Deepak Pathaniaらは、アクリルアミドグラフトキトサンCPAとCuSナノコンポジットを合成し、フッ素系合成抗菌剤オフロキサシン(下図)の制御された伝達に使用した。4)その結果、オフロキサシンのドラッグ伝達の動力学を、pHを変えて行い、ドラッグ伝達効率の最高値85%を得た。またドラッグ放出効率としてはpH2において18時間後で76%の最高効率を観測した。さらに本ナノコンポジットは大腸菌を24時間後に97%殺菌し高い抗菌性を示した。
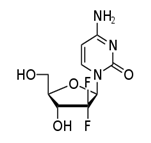
Sanku Mallikらは、フッ素系抗がん剤ゲムシタビン(下図)のがん細胞への細胞質内伝達物質として多機能ポリマーソームを開発した。5)
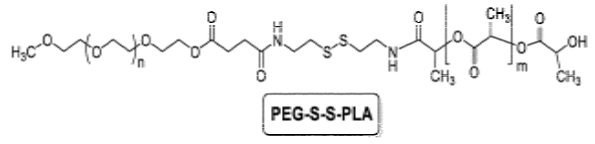
リポソームがドラッグデリバリー物質として広く用いられているが、安定性と遅い徐放性に課題がある。そこで下記の構造のポリマーソームを合成した。PEGの分子量1900とPLA(ポリラクティック酸)の分子量3600(P4)と5800(P5)のポリマーソームが高い徐放性を示した。P5>P4
C. Gopi Mohanらは、5-FUのDDSとして、アモルファスキチンナノ粒子を使用し、捕捉及び輸送効率として47±12%を報告している。因みに同時に試験した非フッ素系抗がん剤の効率はドセタキセルが77±2%、クルクミンが98±1%であった。6)
Jureerut Daduangらは、葉酸を標的剤として用いる胆管がん細胞への5FUの標的デリバリーについて報告している。具体的には金のナノ粒子を、ポリエチレングリコールを用いて5-FUと葉酸(FA)で機能化したもの(AuNPs-PEG-5FU-FA)が5-FUと葉酸だけの場合に比べて、胆管がん細胞M139およびM213への細胞毒性効果として、それぞれ4.76%および7.95%増大した。7)
4、ドラッグデリバリー物質としてのフッ素化合物
目薬ロスポリンA(CsA)のDDSとして半フッ素化アルカン(SFA)が用いられていて、安全で良好な耐用性を有している。疎水性薬をよく溶かし、透明な点眼液をつくることができる。浸透性が改善され、防腐剤不要、目の表面に潤滑性を与える、0.05%のCsAを含むSFAは耐容性があり、FDAで承認された唯一のドライアイ治療薬レスタシスと比べると角膜を超えて水溶性体液中への浸透性が増大していて有望な候補である。Novaliq社の「CyclASo」として登録、フェーズⅠをクリアし、フェーズIIに入っている。8)
半フッ素化アルカン(SFA)、C4F9C5H11(F4H5)やC6F13C8H17(F6H8)は不活性で無害な流体であり親油性ドラッグを溶かす。Priyanka Agarwalらは、SFAの局所的目薬シクロスポリンA(CsA)のドラッグ溶媒としての生物学的利用能や安全性を評価した。9)現行のRestasis(ひまし油にCsAを0.05%溶解させたもの)とエタノール0.5wt%含有F4H5(F4H5E)とエタノール0.5%含有F6H8(F6H8E)にCsAを0.05%溶解させたものと比較した。その結果、短時間ではRestasisは角膜を透過できなかったが、F4H5Eは152.95ng/ml、F6H8では15.12ng/ml透過した。8時間の適用では、Restasisは21.07/ml、F4H5Eでは247.62ng/ml、F6H8Eでは174.5ng/ml透過した。そして角膜毒性は観測されなかった。
Evan Ungerらは、超音波でミクロ泡を発生させるのだが、C3F8、C4F10、C5F12などが安定なミクロ泡を生じさせ、心臓血管へのドラッグデリバリーに有効であることを報告している。10)
5、DDSの代謝安定性評価
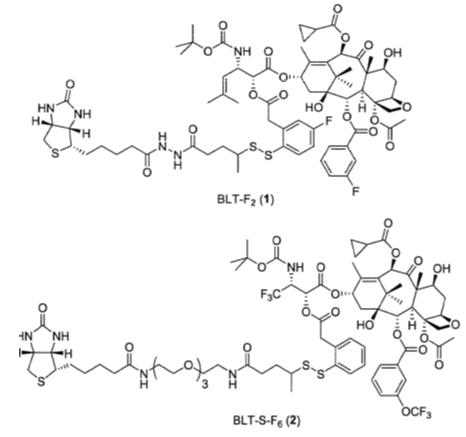
Iwao Ojimaらは、腫瘍を標的としたDDSの代謝安定性評価のための19NMRプローブとして、Fを導入した新規腫瘍標的ドラッグ複合体BLT-F2とCF3を導入したBLT-S-F6を19FNMRプローブとしてデザイン、合成した。(下図)このプローブは、吉草酸、自己崩壊リンカーユニット、フルオロタキソイドからなるが、その安定性と反応性、つまりリンカーの開裂、血症への影響、代謝安定性などを19FNMRでリアルタイムに追跡した。その結果、BLT-F2のフルオロタキソイドの放出は段階的に起こっていることが分かった。これはフェニルアセテートのジスルフィドに対してパラ位のFがリンカー開裂の速度とチオールアセトニゼーション反応に対して大きな影響を与えていることを示唆している。BLT-S-F6はより親水性を高めたものであるが、ヒトの血漿中で自己崩壊ジスルフィドリンカーシステムの安定性と反応性を評価するのに大変有用であることが分かった。そして、ヒトの血漿中での半減期は1週間以上と長いが、タキソイドはスムースに放出する(半減期3時間)ことが分かった。11)
6、おわりに
DDSにおいてフッ素の役割を考察してみると、抗がん剤や合成抗菌剤などのフッ素含有医薬における脂溶性の向上があげられる。つまり医薬にフッ素を導入することはその特異な生理活性のみならずDDSにおける吸収性を高め、放出をより制御しやすくする役割があると考えられる。また、製剤において、親油性ドラッグをよく溶かす半フッ素アルカンを用いることや、泡やエマルションの安定性に寄与する物質としてフッ素化合物を用いることが報告されている。さらにフッ素を導入して、19FNMRによりそのメカニズムを解明し、より有用なDDSを開発することも重要である。今後さらにその重要性が認識されていくことを期待している。
文献
1) 畑中朋美、杉林堅次 日本防菌防黴学会誌43(4) 209 2015
2) 岡田弘晃 日本防菌防黴学会誌 43(3) 157 2015
3) 大矢裕一 日本防菌防黴学会誌 43(1) 41 2015
4) Deepak Pathania et al Materials Science and Engineering C 64(2016) 428
5) Sanku Mallik et al Biomaterials 35(2014) 6482
6) C. Gopi Mohan et al Carbohydrate Polymers 142(2016) 240
7) Jureerut Daduang et al Material Science and Engineering C 60(2016) 411
8) D. M. Dutescu European J of Pharmaceutics and Biopharmaceutics 88(2014) 123
9) Priyanka Agarwal et al Drug Discovery Today21(2016) 977
10) Evan Unger et al Advanced Drug Delivery Reviews 72(2014) 110
11) Iwao Ojima et al Journal of Fluorine Chemistry 171(2015) 148